1 前言
抗体药物因其高特异性、低副作用和治疗效果显著等优势,已成为生物医药领域的核心方向之一。然而,传统抗体药物研发流程长、成本高,尤其是稳定细胞株的构建耗时数月,严重制约了研发效率。近年来,利用化学方法进行瞬转表达的技术的突破性发展,为抗体药物的快速开发提供了全新路径。
在抗体药物研发的早期成药性评估阶段(如分子筛选、初步功能验证、工艺摸索前研究),快速、可靠地获得毫克级至百毫克级重组抗体蛋白至关重要。CHO细胞的化学瞬时转染在这一环节展现出显著优势,特别是在与电转和其他常用宿主细胞(如HEK293)的对比中。
2 不同宿主细胞的差异
2.1 翻译后修饰(PTM)的“金标准”相关性
CHO细胞: 是工业界生产治疗性抗体的绝对主流宿主。其糖基化模式(特别是缺乏α-2,6-唾液酸转移酶,主要产生G0F, G1F, G2F等岩藻糖基化结构)与人源抗体高度相似,且相对稳定、可控。在成药性评估阶段,使用CHO细胞瞬转产生的抗体,其糖型谱、电荷异构体等关键质量属性(CQAs)更接近最终商业化生产的稳定细胞株产品,评估结果更具预测性和参考价值。
HEK293: 糖基化模式与人源更接近(能产生α-2,6-唾液酸化),但其糖型谱通常比CHO更复杂、异质性更高,且表达水平波动可能更大。在CHO主导的生产背景下,HEK293瞬转获得的抗体糖型可能与最终CHO产品存在显著差异,导致早期评估的糖基化相关性质(如ADCC/CDC效应、半衰期、免疫原性风险)预测性降低。
2.2 背景“干净”,内源蛋白干扰少
CHO细胞: 经过长期工程化改造和筛选,用于抗体生产的CHO细胞系(如CHO-K1, CHO-S, DG44, DUXB11)通常内源性蛋白分泌水平较低,尤其是宿主细胞蛋白(HCP)。瞬转表达的抗体在上清中纯度相对较高,有利于下游纯化(即使是小规模)和后续分析(如SDS-PAGE, SEC-HPLC, 结合/功能分析),减少背景干扰。
HEK293: 内源性分泌蛋白(包括HCP)水平通常高于CHO细胞,瞬转收获液背景可能更“脏”,给下游小规模纯化和精确分析带来额外挑战,可能掩盖或干扰对目标抗体本身特性的评估。
2.3 表达稳定性与一致性
在瞬转条件下,优化后的CHO细胞系统通常能提供相对稳定和一致的抗体表达水平(尤其是在同一批次实验内),有利于进行不同候选分子间的平行比较。
HEK293瞬转的表达水平有时波动性较大,批次间差异可能更显著,增加了实验的变异性。
2.4 与下游工艺开发的衔接性
使用CHO细胞进行早期瞬转评估,其表达的抗体在杂质谱(HCP, DNA,糖型等)上更接近后续稳定细胞株的产物。这使得在早期成药性评估阶段(如稳定性、可开发性、初步纯化回收率)获得的数据,对后续工艺开发(如层析填料选择、纯化条件优化)更具指导意义。
HEK293表达产物的杂质谱差异可能导致早期工艺摸索数据外推到CHO平台的可靠性下降。
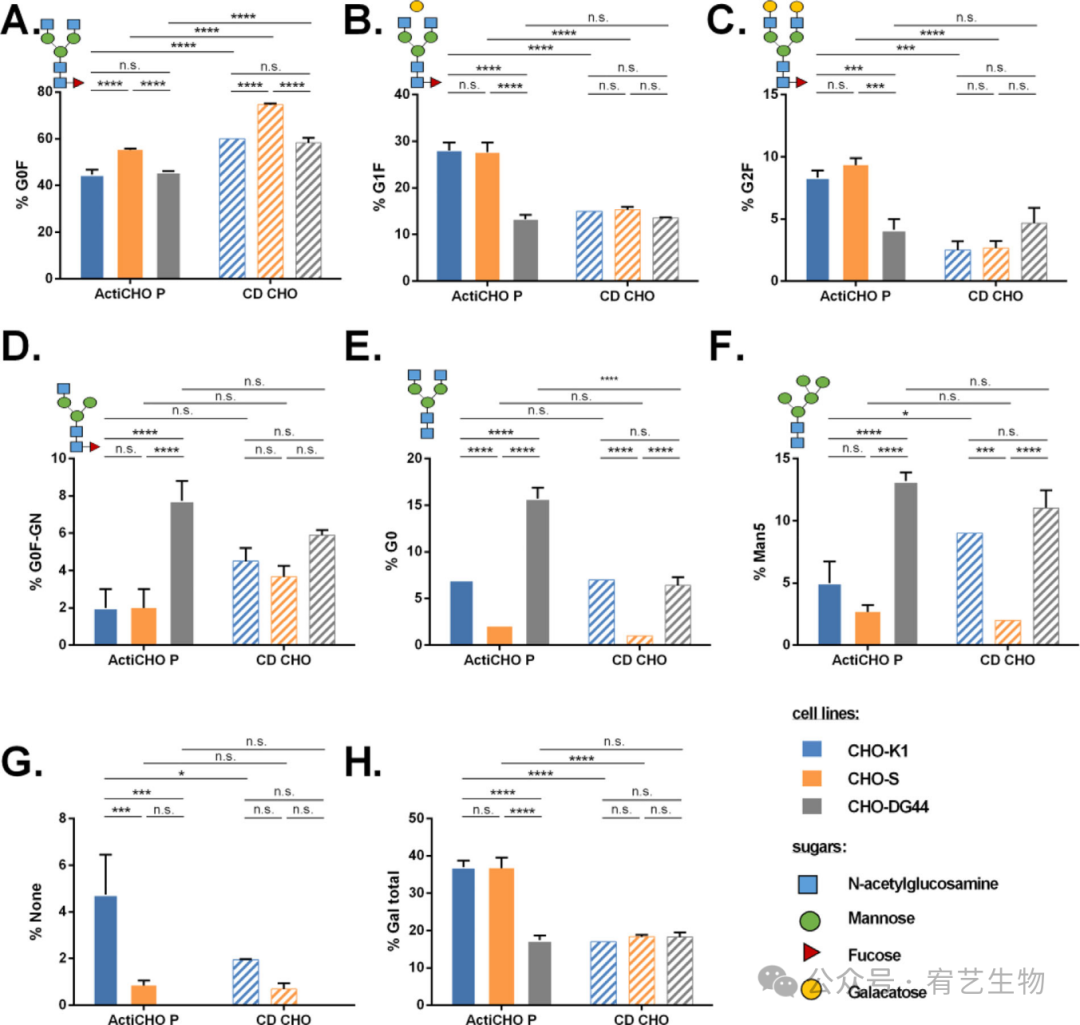
Figure 1. Glycoform distribution of heavy chain of mAb expressed in CHO-K1, CHO-S, and CHO-DG44 fed-batch cultures based on ActiCHO P or CD
CHO media. Antibody quality of (A) G0F, (B) G1F, (C) G2F, (D) G0F-Gn, (E) G0, (F) Man5, (G) non-glycosylated, and (H) total percentage of
galactosylated mAb was analyzed of the harvest product fraction after fed-batch termination. All values represent the mean of three replicate
experiments, the error bars show one standard deviation.
因此,采用稳定表达用宿主细胞进行化转以评估候选分子将降低由于宿主细胞不同带来的评估结果的偏差。
3 相对于电转的优势:省时、省力
3.1 操作简便性与可及性
化学转染: 通常只需将DNA与转染试剂(如PEI)在简单缓冲液中混合,直接加入细胞培养体系即可。操作步骤标准化,易于掌握,在普通细胞培养实验室即可进行,无需特殊设备。
电转: 需要昂贵的电转仪、特定规格的电转杯/板,操作相对复杂(涉及细胞洗涤、重悬、电击参数优化等),对操作人员技术要求更高,通量相对受限。
3.2 细胞活性与状态影响小
化学转染: 优化的化学转染试剂(尤其是现代高分子聚合物如PEI)对细胞膜损伤较小,转染后细胞活性通常较高(>80%),细胞恢复快,更有利于后续培养和蛋白生产。细胞状态更接近正常培养,减少了因转染本身引入的变量。
电转: 高电压电脉冲会对细胞膜造成可逆或不可逆的穿孔,导致瞬时细胞死亡率显著升高(常需优化到可接受水平),细胞需要更长时间恢复,可能影响蛋白表达的总量和质量(如聚集倾向)。
3.3 成本效益高
化学转染: 主要成本是DNA和转染试剂。无需一次性电转耗材(电转杯/板),设备投入低。特别适合大规模、高通量的早期筛选。
电转: 设备成本高,一次性耗材(电转杯/板)成本不菲,限制了其在大量平行实验中的应用。
3.4 通量适应性
化学转染: 极易从6孔板、摇瓶轻松放大到多深孔板、方瓶、甚至小型生物反应器(如50mL - 1L工作体积),实现高通量平行表达和中等规模放大,满足早期评估不同分子、不同工艺条件的需求。
电转: 高通量化(如96孔电转板)通常效率较低、成本高、操作繁琐,更适合小规模(如24孔板以下)或特定细胞类型的转染。大规模放大困难。
3.5 实验条件更接近最终生产环境
化学转染通常在标准的细胞培养容器和培养基中进行,与后期稳定细胞株培养和生产条件更相似,所得产物的特性(如糖基化、电荷异构体)可能更具预测性。
基于上述思考,宥艺推出CHO细胞瞬转套装,可实现CHOZN等CHOK1细胞的千升规模瞬转,最高抗体表达量实现4g/L的瞬时表达量,产量完全满足临床前和临床一期的需求,为加速新药研发赋能。
表1产品说明
产品名称 | 货号 | 说明 |
Trans BM03 | YYT03.001 | 培养基 |
FM02AB | YYFM02AB.02 | 补料 |
CHO enhancer | YYenhancer.001 | 表达增强剂 |
Trans 8 | YYTrans8.001 | 转染试剂 |
4 部分测试数据
图1转染效率超过80%
左为宥艺转染效率,右为常规化转转染效率
图2 CHOZN细胞的化转瞬时表达
图3自主驯化CHO-K1细胞高密度化转瞬时表达
5 产品优势介绍
-更高的表达量:24h即可达到100mg/L以上,72h可达到500mg/L以上;
-更简便的操作方式:1分钟完成化学转染;
-适合大体积瞬转,放大线性好,解决CMC大体积瞬转的难题;
-毒性低,缩短稳定细胞株构建时间;
-工艺简单:可实现7天补料一次;
|
|
https://mp.weixin.qq.com/s/Y7SBKMlDr_yexUjZxuBkAA
|




