宥艺生物部分CHO细胞培养基完成DMF备案
近日,上海宥艺生物科技有限公司(以下简称“宥艺生物”)收到美国食品药品监督管理局(以下简称“FDA”)邮件确认,宥艺生物递交的第一个培养基产品CHO BM04系列产品(备案号:DMF039918)正式完成美国FDA的DMF备案。
宥艺生物其他若干产品均在提交过程中,持续不断的提升用户体验。

什么是DMF备案?
DMF是指药品主文件(Durg Master Files),是持有者递交给FDA的产品信息的存档文件,包含产品在生产过程中用到的工艺、产品主要成分表、质量标准等细节信息,涉及部分保密信息。
为什么做DMF备案?
根据美国联邦食品、药品和化妆品法规定,药品在上市之前申报者必须向FDA提出相关的申请,比如新药注册(NDA)和生物制品许可证申请(BLA)等,并需要提供该药物在安全性、有效性和质量三方面的全部信息,其中涉及到原料药、辅料的相关技术内容,但是准备这些材料无疑会耗费大量的时间和精力,同时原料供应商也不愿透漏自己的技术信息,因此严重影响临床申报的进程。为解决这一问题,FDA建立了DMF体系,原料供应商以DMF文件的形式将所需的技术内容直接交给FDA备案并获得备案编号,药物申报者可以直接使用DMF备案编号来代替申报过程中需要提供有关原料和辅料的具体信息,极大程度上缩短了审查和评估时间。
关注宥艺生物微信公众号:欢迎咨询宥艺产品,宥艺生物将免费提供测试产品。
关于宥艺生物
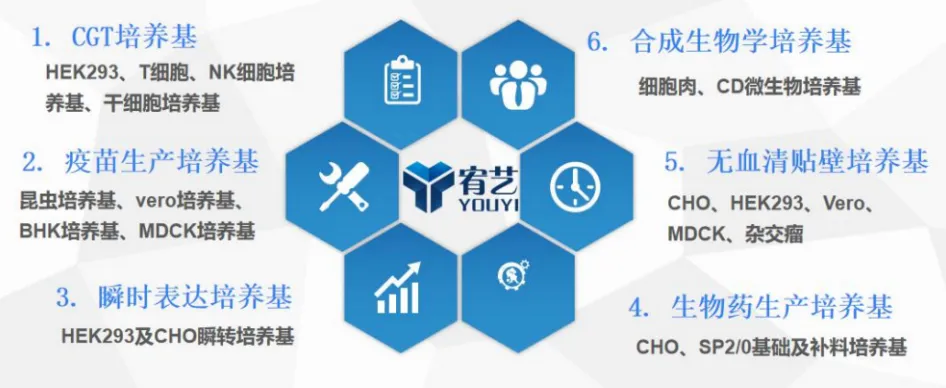
上海宥艺生物科技有限公司成立于2022年3月份,是一家专业的细胞培养基研发及生产供应商涵盖CHO细胞培养基、HEK293培养基、Vero细胞培养基、昆虫细胞培养基、杂交瘤培养基,T及NK细胞培养基和干细胞培养基等。公司目前在苏州市吴江区建有1000m2研发实验室及2000平方按GMP标准建设的生产车间,具备单批次500kg干粉生产能力(针磨)和1000L液体灌装及袋装培养基生产能力。宥艺生物致力于解决未被满足的培养基市场需求及拓展培养基应用领域,不仅仅只在CHO细胞培养基中内卷,经过2年的研发已经建立完善的6大培养基产品线,并在持续的推出具有差异化的培养基产品,比如基于非PEI转染的CHO瞬转试剂盒等:
关注宥艺生物微信公众号:欢迎咨询宥艺产品,宥艺生物将免费提供测试产品。
网址:www.youyimedium.com
邮箱:bd@youyimedium.com
联系电话:18193664815
